Rolando Pérez Rodríguez, director de Ciencia e Innovación del grupo BioCubaFarma, calificó de hito importante que el candidato vacunal Soberana 02, uno de los cinco de la mayor de las Antillas contra la COVID-19, haya recibido la aprobación del CECMED, agencia reguladora nacional, para comenzar la fase III de ensayos clínicos.

Al comparecer en el programa radio-televisivo Mesa Redonda el experto actualizó el estado de los primeros cuatro candidatos cubanos y del quinto, de más reciente incorporación y conocido por Soberana plus, una de las formulaciones iniciales que se evaluaron de Soberana 01 y que será una vacuna de refuerzo, utilizada en pacientes convalecientes del coronavirus.
Esperamos que ahora en marzo el candidato vacunal Abdala reciba la autorización del Centro para el Control Estatal de Medicamentos, Equipos y Dispositivos Médicos (CECMED) para iniciar su fase III, subrayó el especialista.
Refirió que los resultados que muestra el país lo hacen ser el único de América Latina con un candidato en fase III de ensayos clínicos, pues los 16 en ese estado en el mundo son desarrollados por transnacionales farmacéuticas o naciones en vías de desarrollo, como Brasil e India.
Pérez Rodríguez hizo énfasis en los esfuerzos internacionales para obtener una vacuna contra la COVID-19 en tan poco tiempo, pues la fabricación de esos productos es un proceso largo y complejo.
En ese sentido, actualizó que son 308 los candidatos vacunales que se registran en la actualidad, de ellos 81 en ensayos clínicos, mientras los cubanos Soberana 02 y Abdala compondrán el selecto grupo de los que se encuentran en la fase final de prueba.
Un total de 15 vacunas cuentan con autorización de emergencia, la mayoría con un esquema de dos dosis, puntualizó el experto.
Hasta el cuatro de marzo se han administrado 284 millones de dosis de vacunas en el mundo a 116 millones de sujeto; sin embargo, las personas inmunizadas aun no representan ni el uno por ciento de la población, declaró el directivo de BioCubaFarma.

Se refirió a Israel, país en la avanzada para inmunizar a la totalidad de su población, y que tiene más del 20 por ciento de sus ciudadanos vacunados con ambas dosis, por lo cual muestra ya una reducción del 65 al 85 por ciento de los casos positivos al SAR-CoV-2.
Los candidatos que han llegado a fase III han demostrado que inducen anticuerpos neutralizantes, equivalentes a los de los pacientes convalecientes, aquellos que logran vencer la enfermedad y que reportan determinado grado de inmunidad, explicó Pérez Rodríguez.
Las vacunas aprobadas por la Organización Mundial de la Salud para su uso de emergencia reducen del 70 al 90 por ciento la tasa de incidencia de la enfermedad, si bien la OMS plantea que ya el 50 por ciento es un valor significativo.
Sobre Cuba, el experto afirmó que el CECMED ha exigido de manera estricta el cumplimiento de todas las regulaciones en aras de que exista evidencia para pasar a la otra etapa y asegurar además, la seguridad de los voluntarios.
Soberana 02 arribó a Fase III sin comprometer el rigor de sus resultados
El candidato vacunal Soberana 02 comenzó este jueves su Fase III de ensayos clínicos sin comprometer los resultados en términos éticos y regulatorios, afirmó la Doctora en Ciencias Farmacéuticas Dagmar García Rivero, directora de Investigaciones del Instituto Finlay de Vacunas (IFV).

En su intervención en la Mesa Redonda dijo que para avanzar con un candidato vacunal se necesita concluir cada etapa, pero a partir de la flexibilización de los procedimientos regulatorios a nivel mundial se ha podido solapar cada fase y escalar en los procesos productivos.
La también Premio de la Academia de Ciencias de Cuba y Premio Anual de la Salud señaló que ya están producidas las 320 mil dosis de Soberana 02 necesarias para el ensayo clínico, y el sistema productivo ha sido inspeccionado por el Centro para el Control Estatal de Medicamentos, Equipos y Dispositivos Médicos (CECMED), la entidad reguladora.
Refirió que esta etapa convertirá a La Habana en un gran sitio clínico al abarcar unos 44 mil 010 voluntarios de ocho municipios, por lo que cuentan con el apoyo del Ministerio de Salud Pública (MINSAP), la Dirección Provincial de Salud, el Consejo de Defensa Provincial y los Consejos de Defensa Municipales; además de las universidades, en el manejo de datos y la organización.
Soberana 02 es la primera vacuna en Latinoamérica en llegar a la Fase III, dijo García Rivero, y aclaró que este logro de la biotecnología cubana se debe a la alianza estratégica entre muchas instituciones, tanto del Grupo de las Industrias Biotecnológica y Farmacéutica de Cuba (BioCubaFarma) como del MINSAP.
Recordó que nueve meses atrás, en mayo, comenzó a definirse un proyecto de vacuna específica contra el SARS-CoV-2 y en agosto se iniciaron los ensayos clínicos Fase I del candidato vacunal Soberana 01, para luego continuar en octubre con Soberana 02, el más avanzado de los desarrollados en el país.
Detalló que este último empezó el estudio Fase I con 40 sujetos de entre 19 y 59 años de edad, pues en este rango etáreo existen menos riesgos asociados a la vacunación.
La Fase II continúo con 910 sujetos entre 19 y 80 años de edad y durante estas dos etapas no se reportaron eventos adversos graves relacionados con la vacunación.

En cuanto a los indicadores de inmunogenicidad, puntualizó la investigadora que en la primera etapa, luego de la tercera dosis, el 90 por ciento de los sujetos tuvieron anticuerpos neutralizantes y en la segunda, después de dos dosis, resultó el 76 por ciento y al incluir la aplicación de la tercera dosis se prevé alcanzar indicadores mayores.
No obstante emplear plataformas conocidas y alcanzar buenos resultados en cuanto a seguridad e inmunogenicidad en los estudios previos, es preciso arribar a una tercera fase para demostrar la eficacia del fármaco cubano, por lo cual se solicitó el inicio a la entidad regulatoria, dijo García Rivero, quien en 2019 recibiera la condecoración Carlos J. Finlay, máximo reconocimiento a los científicos cubanos.
Destacó que en el programa de desarrollo clínico del IFV, como promotores de la vacuna, la institución no evalúa los resultados de las muestras, sino que los encargados son entidades externas, lo que valida el trabajo realizado de cara a una auditoría de la Organización Mundial de la Salud y a la certificación de nuestras vacunas.
Pasos de la fase III del candidato Soberana 02
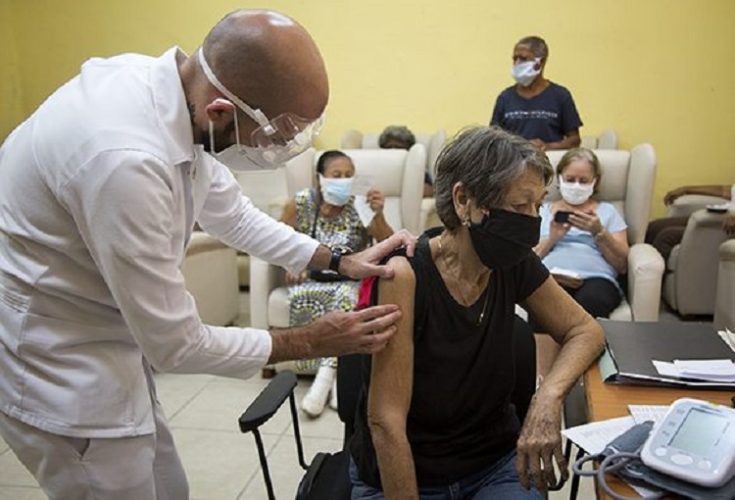
María Eugenia Toledo Romaní, investigadora principal del ensayo clínico del candidato vacunal cubano Soberana 02 contra la COVID-19, que comienza su tercera fase, informó hoy que en la actualidad se les entrega a los sujetos la información para consentir su participación en el estudio.
Este involucrará a 44 mil 010 personas de ocho municipios habaneros escogidos y una vez que se desarrolle ese proceso, los sujetos serán evaluados por el médico de la familia para definir si están aptos para el ensayo, precisó la experta del Instituto de Medicina Tropical Pedro Kourí, al explicar los pasos correspondientes en el espacio informativo Mesa Redonda.

También en la atención primaria se realizará la prueba de anticuerpos con vistas a evaluar si alguna vez la persona estuvo expuesta al SARS-CoV-2 y como consecuencia presenta inmunidad, dijo Toledo Romaní.
Explicó que en cada sitio clínico se hará un cronograma para definir cuándo los seleccionados deben acudir al policlínico, donde serán evaluados por un grupo médico en aras de verificar que continúan cumpliendo los criterios de inclusión; ahí recibirán un código que representa su número en el estudio y el grupo de tratamiento que le corresponde, dato que será secreto al ser un ensayo a ciegas.
Los esquemas de inmunización a emplear son: uno con dos dosis, otro con dos dosis de Soberana 02 y una de refuerzo de Soberana 01, además de un grupo placebo, quienes serán beneficiados con el candidato vacunal una vez que culmine el estudio.
Al vacunarse, las personas serán observadas durante una hora en el sitio clínico por especialistas en manejo de urgencias médicas por si presentan un evento adverso grave, y después seguirán siendo evaluadas en la comunidad por el médico de la familia.
Toledo Romaní explicó que el sujeto tendrá un protocolo de manejo diferenciado si resulta positivo en SARS-CoV-2 en el transcurso de la prueba, y aclaró que las personas pueden en acceder a no seguir como voluntarios del ensayo si lo desean.

Para velar por el cumplimiento de lo establecido se creó un comité de ética ampliado que involucró a todas las facultades de Ciencias Médicas de los municipios que participan en el estudio: Playa, Plaza, Centro Habana, Diez de Octubre, Cerro, La Habana Vieja, La Lisa y Marianao.
La investigadora principal del ensayo clínico de Soberana 02 subrayó que podrán participar las personas de entre 19 y 80 años, y en el caso de las mujeres aquellas dispuestas a no embarazarse durante ese periodo.
Informó que los criterios de exclusión son presentar una enfermedad infecciosa aguda, hipersensibilidad al tiomersal, haberse aplicado en los tres meses previos vacunas que contengan anatoxina tetánica, recibir tratamiento con inmunomoduladores, mujeres en estado de embarazo, puerperio o lactancia y tener enfermedades crónicas descompensadas, aspecto que será diagnosticado por el médico de la familia.
Este ensayo tiene como objetivo demostrar la eficacia del candidato vacunal en la prevención de la enfermedad sintomática causada por SARS-CoV-2, infección que, a casi un año de su aparición en el archipiélago, se ha registrado hasta el momento en 54 mil 085 cubanos. (Tomado de ACN)
Abdala: A las puertas de la Fase III
Junto a Soberana 02, el desarrollo del candidato vacunal Abdala abre puertas para el combate contra la COVID-19. Al respecto, la Dra. Verena Muzio González, directora de Investigaciones Clínicas del Centro de Ingeniería Genética y Biotecnología (CIGB), explicó que se basa en la misma plataforma utilizada para crear la vacuna recombinante contra la Hepatitis B.
“En solo tres meses hemos desarrollado las fases I y II, gracias también a la colaboración entre las entidades científicas”.
Los estudios se diseñaron para probar dos esquemas de vacunación: uno largo y uno corto. El esquema corto incluye tres dosis cada 14 días, mientras que el largo implica recibir la vacuna cada 28 días.
“Esto lo hicimos no solo para probar la eficacia del fármaco, sino para evaluar dos niveles de dosis y tener alternativas ante posibles cambios. Entonces descubrimos que en el esquema corto los mejores resultados los tuvieron las altas dosis”, explicó la investigadora.
Se demostró también que más del 60% de las personas desarrollaron niveles de inhibición. Al terminar la tercera dosis, el 95% tenían anticuerpo incrementados más de cuatro veces en relación al momento del inicio del estudio. “Con estos resultados propusimos comenzar el ensayo en fase III”.

La Dra. Verena Muzio González, directora de Investigaciones Clínicas del Centro de Ingeniería Genética y Biotecnología (CIGB), señaló que en el caso del candidato ABDALA “la estrategia de solapamiento ha permitido que comencemos la fase II tomando una decisión de la fase I, faltando aún algunos momentos para concluirlo, y de este mismo modo ocurrirá con la fase III”.
“Resulta significativo para nuestro país que, el mismo día en que Soberana 02 recibió su autorización para iniciar el ensayo fase III por el CECMED, nosotros estábamos entregando la documentación de solicitud de autorización de ensayo clínico, lo cual demuestra el intenso trabajo de Cuba en el desarrollo de vacunas”, destacó.
El ensayo fase III de Abdala comenzará cuando la autoridad reguladora nacional lo autorice, si bien se espera que sea en este mismo mes de marzo.
“Trabajamos para tener listas todas las condiciones requeridas, para en el momento que hayamos cumplido todas las exigencias del CECMED y este diese su autorización, no tener que esperar”, dijo Munzio González.
Fase III de Abdala: 42 mil sujetos de Guantánamo y Santiago de Cuba
El ensayo fase III de Abdala tendrá varios objetivos. Entre ello, demostrar la eficacia de la vacuna y su capacidad para proteger a los individuos vacunados en una proporción superior a los individuos que reciben el placebo. También busca evaluar la seguridad del inmunógeno, requisito durante todo el desarrollo del producto, al igual que lo relacionado con la respuesta inmune.
Señaló que se prevé incluir en el ensayo a 42 mil sujetos de las provincias de Guantánamo y Santiago de Cuba. Esta última provincia ya venía trabajando en el ensayo fase II por lo que ya existe experiencia y un grupo de investigadores capacitados.
“Coincidentemente, en el momento que empezamos a hacer el trabajo, Santiago de Cuba y Guantánamo junto a La Habana pasaron a ser las provincias con mayor incidencia de casos de la enfermedad en el país, por lo cual decidimos ampliar el ensayo a las mismas”, relató.
El sitio clínico principal es el hospital Saturnino Lora. Es un estudio multicéntrico, controlado con placebo, aleatorizado porque la persona no decide para qué grupo va y a doble ciegas. Están involucrados comités de ética de ambas provincias para la aprobación.
El diseño general del estudio contempla la administración de tres dosis separadas por 14 días. Una vez se obtenga la autorización de la agencia reguladora se inicia el proceso de captación, pre reclutamiento, consentimiento, precisó.
“Tenemos un reto enorme pero factible. Dado lo corto del esquema de vacunación de Abdala, queremos incluir esos 42 mil voluntarios en dos semanas. Tenemos el apoyo de las autoridades del gobierno, del partido, los consejos de defensa de ambas provincias, así como de las direcciones de salud pública y el resto de los involucrados”, dijo.
Pensamos establecer sitios de vacunación con horarios extendidos y existen sitios clínicos en los cuales habrá más de un vacunatorio, agregó. 14 días después de la última dosis comenzamos a evaluar la eficacia del producto.
En Guantánamo se incluyeron 5 áreas de salud que contemplan 12 mil individuos. Mientras, en Santiago de Cuba, además del hospital Saturnino Lora se trabajará en 13 áreas de salud con un alcance de 30 mil sujetos.
“Todo ello es posible también gracias a poder contar con un sistema productivo que, en el caso de Abdala, está integrado por el CIGB, centro productor del ingrediente farmacéutico activo, los laboratorios AICA, para la formulación, llenado y envase que cuenta con las capacidades de escalado necesarias. Todas las vacunas para la fase III ya están producidas”, concluyó. (Tomado de Cubadebate)