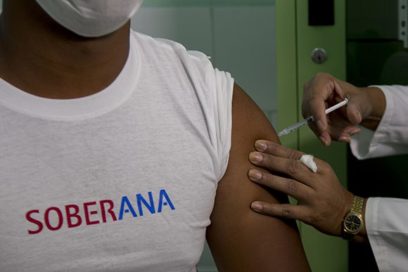
Un estudio Fase I en pacientes convalecientes de COVID-19, con muy bajos títulos de anticuerpos luego de la infección y con riesgo de reinfectarse, avanza en el Instituto de Hematología e Inmunología de la capital, sitio clínico de la investigación, con el candidato vacunal Soberana 01, del Instituto Finlay de Vacunas.

El ensayo comenzó el pasado día 9 de enero con el reclutamiento de 30 voluntarios entre los 19 y 59 años de edad, y continuó con la vacunación el día 16 de enero. En el día de hoy, en consulta de seguimiento, se realizó toma de muestra de sangre para evaluar la respuesta inmune de los participantes.
Hasta el momento, informó el doctor en Ciencias Médicas, Rolando Ochoa Azze, investigador y profesor Titular y consultante del Instituto Finlay de Vacunas (IFV), se han detectado solamente eventos adversos leves y de corta duración.
El experto explicó que se trata de un estudio Fase I, abierto, adaptativo y monocéntrico, para evaluar la seguridad, reactogenicidad y explorar la inmunogenicidad del candidato vacunal profiláctico FINLAY-FR-1A (Soberana 01) anti SARS-CoV-2, en personas convalecientes de COVID-19.
Está concebido para grupos de sujetos que tuvieron un cuadro clínico leve o hayan sido asintomáticos, dijo.
“Pero estas personas tienen una característica: bajos niveles de anticuerpos neutralizantes, y por lo tanto susceptibles de reinfectarse, es decir volver a contraer el coronavirus. Está descrita la posibilidad de reinfección cuando los anticuerpos neutralizantes son pocos. ¿Cuál es la hipótesis científica que estamos manejando?
“Pues que estos individuos que han estado en contacto con el virus SARS-CoV-2 deben de tener células linfocitos B de memoria contra la proteína de la espiga, y por lo tanto nosotros pretendemos estimular esos clones de células B con una sola dosis de refuerzo del candidato vacunal Soberana 01”, explicó el investigador.
En el contexto del ensayo clínico de convalecientes, único ensayo en el mundo que se ha dirigido a este grupo poblacional, hemos seleccionado la formulación de la Soberana 01 más sencilla y al mismo tiempo más segura, acorde a este grupo de población, sostuvo Ochoa Azze.
La seguridad del paciente como premisa

De acuerdo con el doctor Arturo Chang Monteagudo, especialista de I y II grado en Inmunología e investigador principal del ensayo clínico, el estudio, de tener resultados positivo, probablemente de paso a un ensayo clínico posterior con un mayor número de sujetos, para evaluar la inmunogenicidad y lo que sería realmente la eficacia y efectividad del producto.
“El Instituto de Hematología e Inmunología es un centro de el nivel terciario de atención de nuestro país, que en este momento ha sido escogido para la participación en este ensayo clínico”, dijo el experto.
Un ensayo clínico es una investigación en la cual se demuestra que el producto que ha sido preparado por un fabricante es seguro de usar en humanos, y al mismo tiempo, que cumple las funciones para las cuales el fabricante dice que ha sido preparado, precisó.
Por lo tanto— insistió Chang Monteagudo— como investigador principal de este ensayo, tenemos la misión de ponernos del lado del paciente y protegerlos desde el punto de vista de la seguridad del producto; y en esta fase del ensayo clínico específicamente, ir evaluando la inmunogenicidad del mismo.
En este ensayo clínico Fase 1 se incluyeron 30 pacientes cubanos, entre 19-59 años de edad, que han estado en contacto con el virus SARS-Cov-2. Se dividen en tres subgrupos: diez pacientes asintomáticos de COVID-19, diez pacientes que presentaron una COVID-19 ligera, y diez pacientes que fueron positivos a los estudios de anticuerpos.
“Digo pacientes porque son convalecientes, pero todos los que participan en el ensayo clínico son personas voluntarias, ya sanos y negativos al PCR”, sostuvo.
Apuntó el experto que este ensayo clínico Fase 1 se extiende por 28 días, desde el día 0 que se aplica la vacuna, hasta la última evaluación del voluntario que ocurre en el día 28. Siete días antes de comenzar, se hizo una consulta de evaluación del voluntario para determinar si podía quedar incluido en el estudio, dijo.
Chang Monteagudo explicó que de forma convencional en los ensayos clínicos Fase 1 se tratan de escoger personas que sean jóvenes y sanos. La diferencia con este ensayo clínico es que, como estamos trabajando con una población que ha estado en contacto con el virus, se ha permitido que se incluyan en el estudio personas que pudieran tener alguna patología crónica, siempre y cuando la misma esté compensada.
La otra premisa de inclusión es que los porcentajes de inhibición de esos anticuerpos contra el SARS-CoV-2 sean relativamente bajos. Es decir, personas que han estado en contacto con el virus, pero que no han quedado con inmunidad contra el mismo.
Respecto al segumiento del paciente luego de aplicado el candidato vacunal, el especialista destacó que este proceso comienza en el momento mismo de la vacunación.
Cuando el sujeto vuluntario que participa en el estudio recibe la vacuna se vigila activamente durante tres horas posteriores a la administración del producto. Asimismo, se hacen consultas de evaluación y seguimiento a las 24, 48 y 72 horas, se hace una consulta al séptimo día, una al día 14 y otra al día 28; independientemente que durante todo el tiempo que dura el ensayo Fase 1 los voluntarios están en contacto con los investigadores y cualquier evento adverso o situación que ellos presenten, tienen las vías para comunicarse con nosotros y pueden ser atendidos en cualquier momento, precisó.
“Hoy es el día 7 después de la aplicación del candidato vacunal. Estamos en el marco de un ensayo clínico que se encuentra en ejecución, por lo que no podemos dar datos específicos sobre los resultados que se han ido obteniendo. Preliminarmente puedo decir que no se ha reportado ningún evento adverso grave relacionado con la vacuna en ninguno de los voluntarios participantes”, aseguró Chang Monteagudo.
Dosis única
Este ensayo clínico sostiene como premisa que una dosis única de refuerzo con el candidato vacunal Soberana 01 pudiese ser suficiente para estimular los niveles protectores de anticuerpos neutralizantes.
“Es una única dosis, porque esta formulación y la forma de administración del producto se basan en la premisa de que todas estas personas ya han sido vacunadas, pero han sido vacunadas de forma natural por haber estado en contacto con el virus. Por lo tanto, la hipótesis científica que se ha trazado es que una sola dosis de este candidato vacunal puede ser un refuerzo, o de cierta forma, un recordatorio a la inmunidad del individuo que ya había estado en contacto con el virus, por lo que una sola dosis ya puede levantar los niveles de anticuerpos protectores contra la enfermedad”, explicó el doctor Chang Monteagudo.
De acuerdo con el investigador Ochoa Azze, la formulación de la Soberana 01 que se está utilizando en este ensayo de convalecientes ya fue evaluada en un ensayo clínico anterior que se denomina Soberana 01 A. “En ese estudio, se ha demostrado que es un producto seguro, muy inmunogénico, y esta fue una de las razones que tuvimos en cuenta para poder utilizarla en convalecientes; el hecho de que ya había sido probada con anterioridad”, afirmó.
Ciencia hecha entre todos
Aunque el Instituto de Hematología e Inmunología es el sitio clínico que está conduciendo este ensayo, por las características del grupo de voluntarios que han sido incluidos en el estudio, tuvimos que contar con la participación de un grupo de instituciones del Sistema Nacional de Salud y de estudios previos poblacionales, refirió el investigador principal del ensayo clínico.
De acuerdo con Chang Monteagudo, es importante conocer que el Centro Nacional de Genética Médica había desarrollado un estudio en personas convalecientes en la población cubana, el cual “nos ayudó a reclutar personas para este ensayo, conducido además por el Centro Nacional Coordinador de Ensayos Clínicos (Cencec)”.
Por otra parte, el Programa Nacional de Sangre, el Banco de Sangre y el propio Instituto de Hematología e Inmunología han estudiado personas convalecientes en otras investigaciones y acciones clínicas que también nos permitieron reclutar personas, dijo.
“La Escuela Nacional de Salud Pública y el Centro de Inmunoensayo también aportaron a este ensayo. Esta última fue la institución cubana que desarrolló un estuche para detectar anticuerpos en la población, y por lo tanto podíamos contar ya con una preselección de sujetos que, teóricamente, cumplían con los criterios de inclusión de nuestro ensayo”, agregó el doctor Chang.
Proteger a toda la población
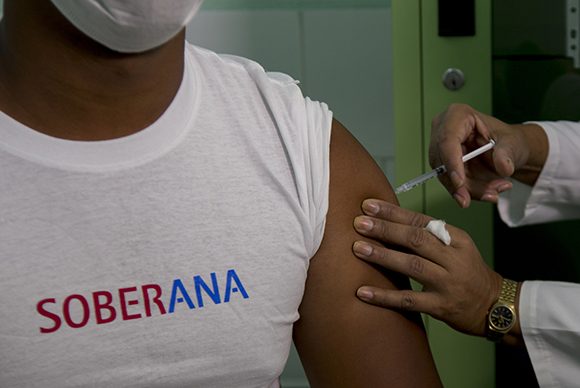
Insistió el profesor Ochoa Azze en que la comunidad científica internacional hay mucha discusión en cuanto a si los convalecientes del SARS-CoV-2 son susceptibles a volverse a reinfectar. “Hay quien considera que quien tuvo la COVID-19 no va a volver a padecerla, y los criterios en ese sentido son muy diversos. Sin embargo, sí se han reportado muchos casos de personas que han padecido la COVID-19 y se han reinfectado incluso con formas mucho más agudas y graves de la enfermedad”, apuntó.
“En Cuba, por las características de nuestro sistema de Salud, nosotros estamos buscando la manera de proteger a toda la población, incluso a los convalecientes. Porque cuando terminen los estudios Fase 2 de las distintas vacunas, culminen los estudios Fase 3, que en el caso de Soberana 02 estamos hablando de 150 000 voluntarios, se autorice el uso de emergencia para algunos grupos poblacionales vulnerables, como es el caso del personal de la salud, las personas mayores de 65 años, el personal del turismo; en ese momento es muy probable que el segmento de personas convalecientes no estén incluidos en estos primeros grupos, y es una población de alto riesgo que hay que proteger. Si se puede demostrar que con una sola dosis es suficiente, estaremos haciendo un aporte importante en relación a la protección de este grupo poblacional, nada despreciable”, consideró el investigador.
¿Cómo avanza Soberana 01?

Según explicaron los expertos, el candidato vacunal Soberana 01 incluyó cinco formulaciones, cada una de las cuales fue estudiada en un Fase I de Ensayo clínico. Algunas de estas formulaciones se basan en el RBD dimérico adsorbidas en gel de hidróxido de aluminio; otras añaden vesículas de membranas externa de meningococo B como adyuvante.
El análisis de estas formulaciones concluyó en diciembre de 2020, pudiéndose constatar la seguridad, la baja reactogenicidad del producto y adecuada inmunogenicidad del candidato, que debe ser corroborado en estudios posteriores. Por los buenos resultados obtenidos, se prevé en febrero comenzar un fase II/III con este inmunógeno.
“Si estudiamos cinco formulaciones es para seleccionar la más óptima, la más adecuada para utilizar en la población, y por supuesto, esta vacuna continuará su desarrollo clínico al igual que la Soberana 02”, puntualizó el doctor Ochoa Azze.
Agregó que en todos los ensayos clínicos de las vacunas contra el coronavirus que se desarrollan en Cuba, específicamente de la serie Soberana (cinco formulaciones de Soberana 01 y dos formulaciones de Soberana 02), a diferencia de otras vacunas— en las cuales son personas completamente sanas, y se hacen criterios de inclusión y de exclusión para definir lo que es una persona sana— se está incluyendo individuos que tengan enfermedades crónicas, siempre y cuando estén controladas. Por ejemplo, un hipertenso puede participar en estos estudios, en los actuales y los que se harán; un diabético puede participar, siempre y cuando los valores de glicemia estén en rango adecuado para sus características personales.
Ello es una fortaleza, en tanto así los ensayos no solo responden más a las características de la población cubana, sino que permite acelerar el desarrollo clínico. Está demostrado que la evolución a formas más graves de la COVID-19 ocurre generalmente cuando coexisten en el paciente comorbilidades. “Normalmente con vacunas contra otros agentes se trabaja en voluntarios sanos y luego en otros estudios se evalúan otras poblaciones. Un proceso que dura años, lo cual no podemos permitirnos en estas circunstancias”, subrayó.
(Tomado de CubaDebate)