Los ensayos clínicos de los dos candidatos vacunales desarrollados en el Centro de Ingeniería Genética y Biotecnología (CIGB) de Cuba concluyeron el ciclo corto de su fase I.

Así lo informaron líderes de los estudios realizados para ambos candidatos: Mambisa, aplicado principalmente por la vía nasal y Abdala por la intramuscular.
La gerente del ensayo, Miladys Limonta, declaró que el primero ya culminó el ciclo corto del estudio, estipulado para el día cero, 14 y 28.
Este candidato emplea como antígeno la proteína AgsHB del virus de la hepatitis B.
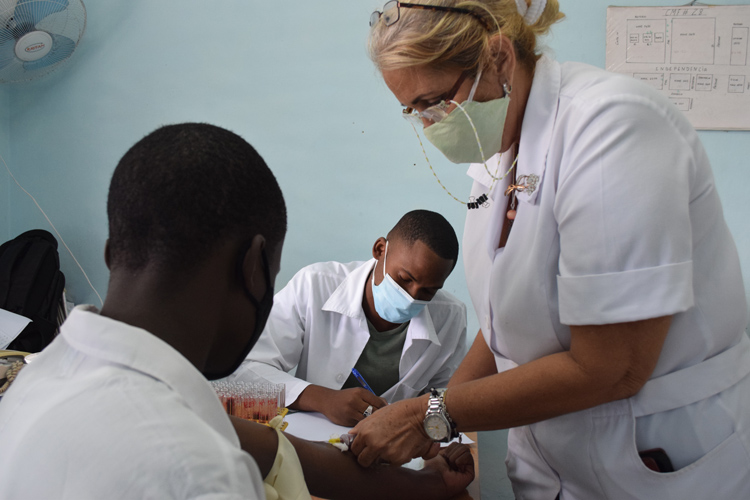
Con una muestra de 88 voluntarios, las primeras inmunizaciones realizadas con Mambisa comenzaron el 7 de diciembre en el hospital Carlos J. Finlay de La Habana.
Los voluntarios están divididos en cuatro grupos, en los cuales se analizarán las vías de administración intramuscular e intrasanal, explicó Limonta.
Después de este primer tiempo, señaló, se pudo constatar la seguridad del fármaco, pues solo se produjeron reacciones adversas leves.
De acuerdo con la experta, al terminar la evaluación de la entidad reguladora, los ensayos pasarían al ciclo largo de estudio, que comprende los días cero, 28 y 56.
El segundo candidato que desarrolla el CIGB, Abdala, también culminó el ciclo corto, en el hospital Saturnino Lora de la provincia de Santiago de Cuba, al oriente del país.
Los 132 voluntarios que integran este estudio han recibido, por vía intramuscular, dos dosis del candidato vacunal y placebo.
El inicio de los ensayos clínicos para Mambisa y Abdala se autorizó el pasado 27 de noviembre por la Autoridad Reguladora de Medicamentos, Equipos y Dispositivos Médicos de Cuba.
Por su parte, en el municipio Plaza de la Revolución comenzó la segunda etapa de ensayo clínico de Soberana 02,desarrollado por el Instituto Finlay de Vacunas.
Unos 405 voluntarios recibirán la primera dosis en el Policlínico 19 de Abril, mientras que más de 100 ya fueron vacunados en la Clínica Uno de La Lisa, al oeste de La Habana.
Este estudio responde a la ampliación de la fase II del candidato vacunal surgido en el Instituto Finlay de Vacunas ante la situación de emergencia global generada por la pandemia de COVID- 19 y que pretende superar las 800 personas vacunadas en esta etapa con el objetivo de verificar los estudios científicos.
El 2 de noviembre último se inició la primera etapa de la fase uno de Soberana 02 con la inclusión de 40 voluntarios y los resultados preliminares del estudio demostraron la efectividad del fármaco cubano. Este fármaco consiste en una suspensión inyectable intramuscular que contiene el dominio de unión al receptor de la proteína S1, conjugado convalentemente al toxoide tetánico absorbido en gel de hidróxido de aluminio.
El ensayo incluye a adultos entre 19 y 80 años de edad, residente en el territorio nacional.
Una vez concluida esta fase dos, se prevé el avance del candidato hacia una fase tres que incluirá alrededor de 150 mil personas.
(Con información de ACN)